タンパク質翻訳に不可欠な転移RNA(transfer RNA, tRNA)は、複雑多彩な転写後化学修飾を受けています。この修飾は、種を超えて保存されており、原核生物からヒトまですべての生物において認められます。このことから、tRNA修飾は、生物にとってtRNAの機能に必須であることが分かります。これまで細菌や酵母を用いてtRNA修飾の研究は盛んに行われてきました。一方、ヒトに対する研究はあまりされていませんでした。その理由は、tRNA修飾異常が疾患発症に繋がるのか不明であったからです。例えば、遺伝子変異やDNAやヒストン蛋白の化学修飾などは、疾患発症との関連が明らかになった以降、網羅的に変異や修飾を調べる研究が世界中で精力的に研究が進められています(オミックス研究)。
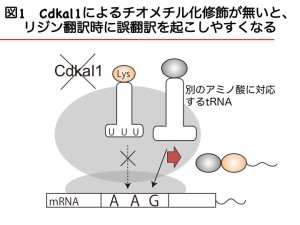 我々は、tRNA修飾異常が疾患発症につながることを最初に報告しました。それが2型糖尿病です。Cdkal1は、2型糖尿病と最も相関のある危険因子の一つです。Cdkal1遺伝子のある塩基に変異があると、2型糖尿病を発症しやすいことがオミックス研究で明らかになりました。しかし、Cdkal1の生理機能は不明でした。我々は、Cdkal1がリジンに対応するtRNAの37番目のアデノシンをチオメチル化する修飾酵素であることを突き止めました。mRNAのコドン配列の一つであるAAGは、アミノ酸のリジンをコードします。AAGの場合、相補的tRNAであるtRNALys(CUU)によりリジンが転移される場合もありますが、生物はtRNALys(UUU)も用います。この場合、コドンの3字目とアンチコドンの1字目は相補的でないので結合しません。すなわち2対の核酸のみで結合することになります。そうすると、理論上tRNALys(UUU)だけでなくtRNAAsn(AUU)あるいはtRNAAsn(GUU)でも結合できることになります。しかし、tRNAAsn(AUU)やtRNAAsn(GUU)が結合すると、リジンがアスパラギンに置換し、誤翻訳が生じてしまいます。37番目のアデノシンがチオメチル化修飾されると、mRNA上のコドン配列の第一ヌクレオチドに結合することが結晶構造解析により明らかになりました(図1)。この結合により、誤翻訳を防止しているのであります。
我々は、tRNA修飾異常が疾患発症につながることを最初に報告しました。それが2型糖尿病です。Cdkal1は、2型糖尿病と最も相関のある危険因子の一つです。Cdkal1遺伝子のある塩基に変異があると、2型糖尿病を発症しやすいことがオミックス研究で明らかになりました。しかし、Cdkal1の生理機能は不明でした。我々は、Cdkal1がリジンに対応するtRNAの37番目のアデノシンをチオメチル化する修飾酵素であることを突き止めました。mRNAのコドン配列の一つであるAAGは、アミノ酸のリジンをコードします。AAGの場合、相補的tRNAであるtRNALys(CUU)によりリジンが転移される場合もありますが、生物はtRNALys(UUU)も用います。この場合、コドンの3字目とアンチコドンの1字目は相補的でないので結合しません。すなわち2対の核酸のみで結合することになります。そうすると、理論上tRNALys(UUU)だけでなくtRNAAsn(AUU)あるいはtRNAAsn(GUU)でも結合できることになります。しかし、tRNAAsn(AUU)やtRNAAsn(GUU)が結合すると、リジンがアスパラギンに置換し、誤翻訳が生じてしまいます。37番目のアデノシンがチオメチル化修飾されると、mRNA上のコドン配列の第一ヌクレオチドに結合することが結晶構造解析により明らかになりました(図1)。この結合により、誤翻訳を防止しているのであります。
インスリンは、プロインスリンから2箇所で切断され作られるペプチドホルモンです。ヒトのインスリンには2つのリジンがあり、その一つは、この切断箇所に位置します。すなわち、もしこのリジンで誤翻訳が生じるとプロインスリンからインスリンに切断されない異常なインスリンが膵β細胞内に蓄積されると考えられます。我々は、膵β細胞特異的にCdkal1を欠損させたマウスを作製しました。このマウスは、切断されない異常なインスリンが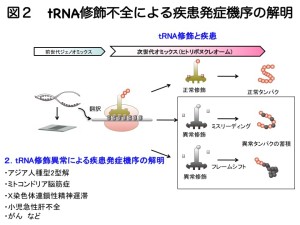 膵β細胞内に蓄積し、その結果、小胞体ストレスが引き起こされることが分かりました。さらに、このマウスに高脂肪食を与えると、異常なインスリンがさらに蓄積し、やがて2型糖尿病を発症することを明らかにしました。我々は、Cdkal1の酵素活性が低下していても、誤翻訳を引き起こさない薬剤の開発をしております。現在、この薬剤が2型糖尿病患者に有効であるか、臨床試験を実施しております。
膵β細胞内に蓄積し、その結果、小胞体ストレスが引き起こされることが分かりました。さらに、このマウスに高脂肪食を与えると、異常なインスリンがさらに蓄積し、やがて2型糖尿病を発症することを明らかにしました。我々は、Cdkal1の酵素活性が低下していても、誤翻訳を引き起こさない薬剤の開発をしております。現在、この薬剤が2型糖尿病患者に有効であるか、臨床試験を実施しております。
我々は、tRNA修飾の異常が2型糖尿病だけでなく、様々疾患の発症に繋がることを明らかにしております(図2)。現在。これら疾患の発症機構の解明を行っており、将来、治療薬開発に繋げたいと考えております。tRNA修飾異常と疾患発症に関する研究は、我々が最初に始めた研究であり、今後も本研究分野をリードしていきたいと思います。
【参考論文】
1. Lamichhane, T., et al. Lack of tRNA-i6A37 modification causes mitochondrial-like metabolic deficiency in S. pombe by limiting activity of cytosolic tRNATyr, not mito-tRNA. RNA 22, 583-596, 2016.
2. Wei, F.-Y., et al. Cdk5rap1-mediated 2-methylthio modification of mitochondrial tRNAs governs protein translation and contributes to myopathy in mice and humans. Cell Metab. 21, 428-442, 2015.
3. Zhou, B, et al. Identification of a splicing variant that regulates type 2 diabetes risk factor CDKAL1 level by a coding-independent mechanism in human. Hum. Mol. Genet. 23, 4639-4650, 2014.
4. Xie, P., et al. Quantitative PCR measurement of tRNA 2-methylthio modification for assessing type 2 diabetes risk. Clin. Chem. 59, 51-59, 2013.
5. Wei, F.Y., et al. Deficit of tRNALys modification by Cdkal1 causes the development of type 2 diabetes in mice. J. Clin. Invest. 121, 3598-3608, 2011.








